Introducere
Una dintre cele mai importante realizări ale științei secolului XXI constă în încercarea de-a studia și de-a înțelege ființa umană într-un mod holist. Desigur că încă există o mulțime de așa-ziși oameni de știință care văd ființa umană ca pe o mașinărie (poate că omul a fost creat după chipul și asemănarea mașinăriilor, la fel cum creierul a fost creat după chipul și asemănarea calculatorului?) izolată de mediul extern (ce ironie), de propriile emoții și de propriul spirit, care poate fi reparată (nu vindecată) doar prin înlocuirea/eliminarea părților sale componente sau printr-o pilulă magică de tipul somei din „Minunata lume nouă”, însă această atitudine reducționistă începe ușor să dispară făcând loc unei noi (sau vechi?) paradigme în care ființa umană este înțeleasă ca un întreg ce aparține unui întreg mai mare.
Să fim totuși atenți și să ne protejăm de spiritopupul de tip superficialisto-capitalisto-mercantil al societății (post)moderniste care confundă vindecarea (și realitatea spirituală a) ființei umane cu o rețetă de shaorma fericită cu gândire pozitivă și sos de bălării energetice, în speranța că această schimbare de paradigmă din comunitatea științifică ne-ar putea aduce ceva mai aproape de lumină (precum bețivul care caută moneda pe strada luminată, deși a pierdut-o pe cea neiluminată, cum spun Leader și Corfield) și adevăr (cu a mic). În rândurile următoare vă voi prezenta o serie de explicații (materialiste) referitoare la interconexiunea dintre sistemele organismului uman având în vedere relația dintre bacteriile din microbiomul intestinal și depresie.
Înainte să încep(em) aș mai adăuga pe scurt următoarele lucruri: a) în text există note de subsol pe care le-am adăugat pentru a facilita procesul de citire și pentru a vă oferi rapid acces la definiții, explicații suplimentare sau la trimiteri către alte articole științifice care să contribuie la înțelegerea fenomenelor respective; b) am optat să păstrez numele bacteriilor din microbiomul intestinal în limba engleză, fiindcă pentru o mulțime dintre acestea nu există un echivalent propriu-zis în limba română; c) articolul este departe de a fi unul exhaustiv; d) la ceva timp după ce am ales titlul articolului am realizat că am trăit o criptomnezie (cum i-ar spune Jung) și că de fapt am reținut o parte din titlul articolului lui Daniels et al. (2017), motiv pentru care meritul (cel puțin parțial) pentru acest titlu îi revine cercetătorului respectiv și colegilor săi; e) mult spor la citit!
Depresia: definiție și caracteristici
Termenul de depresie poate fi utilizat pentru a face referire la 1) o stare afectivă negativă caracterizată de sentimente de tristețe, nemulțumire, deznădejde și/sau pesimism care poate varia ca intensitate (de la ușoară la severă) și care poate interfera cu activitățile din viața de zi cu zi, fiind asociată cu apariția unor schimbări fiziologice, cognitive și/sau sociale precum modificarea somnului, a comportamentului alimentar, retragerea din activitățile sociale, dificultăți de concentrare și/sau de luare a unor decizii, lipsă de energie și/sau de motivație; 2) orice formă de tulburare depresivă (American Psychological Association, 2015).
Apariția depresiei este asociată cu dereglarea activității axei hipotalamo-hipofizo-corticosuprarenale (HHC) [1][2] (Mikulska et al., 2021), cu anomalii structurale, funcționale și moleculare la nivelul sistemului nervos central (SNC) (Zhang et al., 2018), cu diminuarea nivelurilor de factori neurotrofici (ex. factorul neurotrofic de dezvoltare a creierului [FNDC]) [3] și de monoamine (Unal & Moustafa, 2021), cu supraactivarea, activarea continuă/inadecvată a sistemelor inflamatorii ale organismului (Lazary et al., 2021), cu dezvoltarea neuroinflamației cronice (Leonard, 2018), cu acetilarea și metilarea histonelor [4] (Sun et al., 2013) și cu modificări la nivelul microbiomului intestinal [5] (Sanada et al., 2020; Nikolova et al., 2021).
Depresia este una dintre cauzele principale de dizabilitate la nivel mondial (COVID-19 Mental Disorders Collaborators [C19MDC], 2021) și un factor de risc pentru comportamentul suicidar (Park & Hong, 2018) care produce aproximativ 700.000 de decese anual și care constituie cea de-a patra cauză a morții în cazul persoanelor cu vârste cuprinse între 15 și 19 ani (World Health Organization [WHO], 2021).
Prevalența depresiei
Dacă înainte de anul 2020 prevalența depresiei la nivelul populației generale era cuprinsă între aproximativ 10% (Lim et al., 2018) și 15% (Lam, 2018), în perioada pandemiei de SARS-CoV-2 aceasta a căpătat proporții mult mai mari. Anumiți autori (Bueno-Notivol et al., 2021) indică o prevalență de 7 ori mai mare la nivelul populației generale în anul 2020 în comparație cu anul 2017 (25% vs. 3.4%) [6], alături de o creștere de aproximativ 27.6% a numărului de cazuri de tulburare depresivă majoră (TDM) în comparație cu anii precedenți (C19MDC, 2021).
Prevalența depresiei pare să fie dependentă de gen, fiind mai mare în rândul persoanelor de sex feminin în comparație cu persoanele de sex masculin [7] (American Psychiatric Association, 2016). Acest lucru pare să fie valabil cel puțin în cazul adolescenților (Salk et al., 2017), fiindcă prevalența tinde să fie mai mare în cazul persoanelor de sex masculin înainte de atingerea pubertății (Cyranowski et al., 2000) și tinde a se stabiliza pe parcursul perioadei adulte (Salk et al., 2017).
Ce sunt microbiota și microbiomul?
Termenul de microbiotă se referă la ansamblul de microorganisme prezente într-un mediu definit (specific), în timp ce termenul de microbiom este utilizat pentru a descrie întregul habitat care include microorganismele (bacterii, arhee, eucariote inferioare/superioare și virusuri), genomul acestora și condițiile din mediul înconjurător [8] (Marchesi & Ravel, 2015).
Microbiomul este o comunitate microbiană care ocupă un habitat specific și care are proprietăți fizio-chimice distincte, fiind un micro-ecosistem dinamic și interactiv care face parte dintr-un macro-ecosistem (ex. organismul uman) și care îndeplinește roluri esențiale pentru funcționarea și sănătatea acestuia (Berg et al., 2020).
Microbiomul intestinal: definiție și caracteristici
Microbiomul intestinal poate fi înțeles ca un ansamblu de bacterii, arhee, fungi și virusuri care colonizează tractul gastrointestinal, numărul total al acestora fiind estimat la 1014 adică la o sută de trilioane de microorganisme în cazul ființei umane (Thursby & Juge, 2017; Berg et al., 2020). Din acest motiv microbiomul intestinal este uneori înțeles ca un superorganism (Rinniella et al., 2019) sau ca un „organ ignorat” (Cheung et al., 2019). Organizarea taxonomică a bacteriilor din microbiom se realizează în funcție de încrengătură, clasă, ordin, familie, gen și specie (Rinniella et al., 2019).
Deși numărul total de încrengături pare să varieze în literatura de specialitate, unii autori vorbind despre 118 încrengături (Berg et al., 2020) sau de mai mult de 160 de încrengături (Rinninella et al., 2019), cele mai multe dintre cele care au fost descoperite până în prezent nu beneficiază de nici un fel de descriere propriu-zisă (Berg et al., 2020). Cunoaștem totuși că Firmicutes și Bacteroidetes constituie încrengăturile dominante din microbiomul intestinal uman (Armugam et al., 2011) și că există aproximativ 1.800 de genuri și peste 40.000 de specii de bacterii (Evrensel & Ceylan, 2018) care pot avea atât efecte benefice, cât și efecte patogene [9] la nivelul gazdei (Rinniella et al., 2019).
Rolul bacteriilor din microbiomul intestinal în funcționarea organismului uman
Bacteriile din microbiomul intestinal sunt responsabile de procesul de digestie care se realizează prin extragerea, sintetizarea și absorbția nutrienților și metaboliților (ex. lipide, vitamine, amino acizi etc.) din mâncarea pe care o consumăm (Rinniella et al., 2019), fiind astfel implicate în producția de acizi grași cu lanț scurt și amino acizi esențiali, în procesul peristaltic, precum și în metabolizarea și sintetizarea neurotransmițătorilor și a neuropeptidelor (Simpson et al., 2020a).
Ele sunt responsabile și de împiedicarea procesului de colonizare a bacteriilor patogene prin metabolizarea nutrienților, producția de bacteriocine [10], menținerea integrității epiteliului intestinal, modificarea pH-ului, secreția de peptide antimicrobiene [11] și prin efectele pe care le produc la nivelul căilor de semnalizare celulară (Rinniella et al., 2019).
Axa intestin-creier
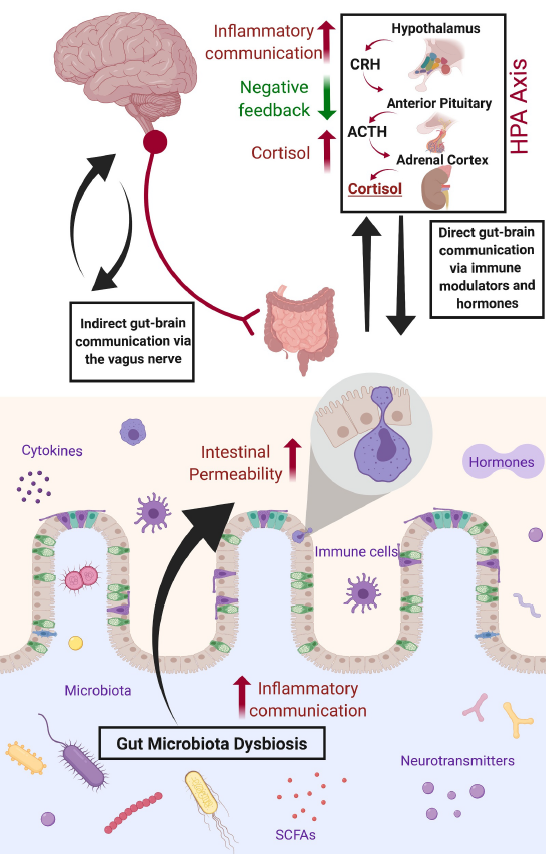
Între microbiomul intestinal și sistemul nervos central (SNC) există o comunicare bi-direcțională care se realizează prin intermediul mecanismelor de semnalizare endocrină, nervoasă și imună ce poartă denumirea de axă intestin-creier (eng. „gut-brain axis”), compoziția și funcțiile microbiomului intestinal putând fi afectate de activitatea cerebrală prin intermediul sistemului nervos autonom (SNA) care poate modifica tranzitul intestinal prin secreție, motilitate intestinală regională și permeabilitate intestinală (Barandouzi et al., 2020).
Axa intestin-creier implică un proces de comunicare între sistemul imunitar și cel endocrin care se realizează prin intermediul citokinelor [12], a proteinelor de fază acută [13], a neurotransmițătorilor și a hormonilor (Simpson et al., 2020a). Un alt proces de comunicare specific axei intestin-creier care se realizează prin intermediul nervului vag și a fibrelor aferente viscerale [14][15] are loc între SNC și sistemul nervos enteric (SNE) [16][17] (Simpson et al., 2020a).
Relația dintre bacteriile din microbiomul intestinal și axa HHC
Bacteriile care colonizează tractul intestinal sunt implicate în procesul de dezvoltare și funcționare a axei HHC (Simpson et al., 2020b). Expunerea la stres (în special cronic) [18] este asociată cu alterarea barierei gastrointestinale, cu creșterea permeabilității intestinelor și cu apariția autoimunității ca urmare dereglării activității axei HHC și a eliberării (cronice) de catecolamine în organism care pot diminua (cel puțin în modelele realizate pe șoareci de laborator) numărul de Lactobacilli, Bacteroidetes și Clostridium și care pot crește numărul de bacterii gram-negative (Misiak et al., 2020).
Modalitatea de funcționare a axei HHC afectează și SNE care este implicat în procesul de inervare a intestinelor (Daniels et al., 2017). Așadar, stările proinflamatorii ale organismului pot produce modificări la nivelul compoziției microbiomului intestinal, la fel cum acesta din urmă poate determina creșterea nivelurilor de cortisol și a inflamației în organism (Simpson et al., 2020b).
Relația (teoretică) dintre bacteriile din microbiomul intestinal și depresie
Încă din perioada perinatală (Evrensel & Ceylan, 2018) bacteriile din microbiomul intestinal sunt direct implicate în dezvoltarea și menținerea homeostaziei și a funcțiilor celulelor imunitare înnăscute și dobândite (adaptative) (Rinniella et al., 2019). Celulele sistemului imunitar produc citokine (precum interleukina-6 (IL-6) [19], interleukina-1β (IL-1β) [20] și factorul de necroză tumorală TNF-alfa (TNF-α) [21]) și modulează funcțiile limfocitelor T-helper 1 (Th1) [22].
Natura interacțiunii dintre microbiomul intestinal și mucoasa intestinală influențează producția de citokine și chemokine [23] pro/antiinflamatorii, cum ar fi interleukina-8 (IL-8) [24], interleukina-10 (IL-10) [25] sau factorul de creștere transformat β (TGF-β) [26] (Evrensel & Ceylan, 2018). Aceste citokine/chemokine pro/antiinflamatorii pot influența în mod diferit producția de proteine de fază acută la nivelul celulelor periferice, ceea ce poate conduce la creșterea/diminuarea inflamației sistemice de grad redus în organism (Lazary et al., 2021).
Disbioza (vezi nota [8] pentru definiție) poate contribui astfel la creșterea nivelului de citokine, de endotoxine și la sintetizarea moleculelor bioactive (Evrensel & Ceylan, 2018; Misiak et al., 2020). Citokinele (ex. IL-6, TNF-α etc.) pot altera motilitatea gastrointestinală, permeabilitatea intestinală și proteinele care se regăsesc în joncțiunile strânse [27] ale tractului digestiv (Simpson et al., 2020a) și pot pătrunde prin bariera hematoencefalică ducând la hiperactivarea axei HHC (Misiak et al., 2020).
Endotoxinele (lipopolizaharidele) [28][29] pot crește permeabilitatea epiteliului intestinal, ceea ce le permite să intre în circulația sanguină, să crească nivelurile de citokine și să (hiper)activeze axa HHC (Evrensel & Ceylan, 2018; Misiak et al., 2020) ducând la apariția inflamației cronice la nivelul SNC (Simpson et al., 2020b).
Pentru că activitatea axei HHC afectează SNE (Daniels et al., 2017) prin intermediul conexiunii cu nervul vag și cu fibrele aferente viscerale (Simpson et al., 2020a), interacțiunea dintre microbiomul intestinal și gazdă poate afecta capacitatea de auto-reînnoire, diferențiere și regenerare a celulelor stem și a celulelor progenitoare la nivelul SNE și al SNC (Misiak et al., 2020).
O parte din microorganismele care se regăsesc în microbiomul intestinal pot produce și consuma anumite tipuri de neurotransmițători (Strandwitz, 2018), pot transporta catecolamine și pot afecta disponibilitatea triptofanului [30] (Misiak et al., 2020). Citokinele proinflamatorii care apar ca reacție a răspunsului imunitar mediat de microbiom determină eliberarea de norepinefrină și de enzime responsabile de convenrtirea levodopa [31] în dopamină și noradrenalină, precum și de metabolizarea monoaminelor (Daniels et al., 2017).
Enterocitele [32] permit celulelor dendritice subepiteliale să-și extindă dendritele în lumenul intestinal și să ia contact cu microorganismele care-l populează și cu metaboliții lor, aceștia din urmă fiind ulterior preluați de celulele dendritice sub formă de vezicule lipoproteice (exozomi) (în interiorul cărora se află nutrienți, endotoxine și genomi bacterieni) care sunt apoi transformate la nivelul nodulilor limfatici în celule T, ceea ce permite metaboliților bacteriilor și acizilor nucleici să intre în contact cu neuronii (Ecrensen & Ceylan, 2018).
De asemenea, nucleul tractului solitar (care se regăsește în măduva spinării) primește semnale de la nervul vag și activează axa HHC prin intermediul neuronilor noradrenergici (Misiak et al., 2020). Toate aceste procese constituie posibile explicații ale modalităților de interacțiune dintre bacteriile din microbiomul intestinal și SNC care sunt asociate cu apariția depresiei.
Rezultatele studiilor referitoare la disbioză în depresie
Dincolo de modelele teoretice, mai multe recenzii sistematice și meta-analize au arătat că există diferențe semnificative la nivelul diversității, abundenței și echilibrului bacteriilor din microbiomul intestinal în cazul persoanelor care suferă de depresie [33][34] în comparație cu grupurile de control, însă rezultatele sunt inconcludente (Cheung et al., 2019; Barandouzi et al., 2020; Sanada et al., 2020; Nikolova et al., 2021).
O recenzie sistematică a arătat că cea mai mare diferență taxonomică este înregistrată în încrengătura Firmicutes (Cheung et al., 2019), iar o altă recenzie a arătat că rezultatele sunt inconsistente în ceea ce privește abundența Firmicutes, Bacteroidetes și Proteobacteria, dar că există o abundență crescută de Actinobacteria și Fusobacteria (Barandouzi et al., 2020).
Pe de altă parte, rezultatele unei meta-analize au arătat că există inconcludențe în ceea ce privește toate încrengăturile menționate anterior (Sanada et al., 2020), acest lucru fiind confirmat parțial și de o altă meta-analiză ale cărei rezultate au arătat că cu excepția Actinobacteria care înregistrează o abundență crescută toate celelate diferențe la nivelul încrengăturilor sunt inconsistente (Nikolova et al., 2021).
Diferențe taxonomice la nivelul familiei
La nivelul familiei rezultatele rămân preponderent inconsistente. Anumiți cercetători au descoperit o abundență crescută de Actinomycineae și o abundență scăzută de Veillonellaceae, Prevotellaceae și Sutterellaceae (Barandouzi et al., 2020; Sanda et al., 2020), în timp ce alți cercetători au descoperit că abundența de Prevotellaceae este scăzută, dar că abundența în cazul Actinomycineae, Veillonellaceae și Sutterellaceae este inconsistentă (Nikolova et al., 2021). Au fost înregistrate și niveluri scăzute ale Bacteroidaceae, Oscillospiraceae, Marniabilaceae și Chitinophagaceae (Barandouzi et al., 2020), însă în altă meta-analiză nivelurile de Bacteroidaceae și Oscillospiraceae au rămas inconsistente (Nikolova et al., 2021).
Unii cercetători (Barandouzi et al., 2020) au înregistrat și o abundență crescută de Coriobacterineae, Bifidobacteriaceae Clostridiales incertae sedis XI, Porphyromonadaceae, Clostridiaceae, Lactobacillaceae, Streptococcaceae, Eubacteriaceae, Thermoanaerobacteriaceae, Fusobacteriaceae, Nocardiaceae și Streptomycetaceae. Rezultatele respective au fost doar parțial replicate de alți cercetători care au descoperit o abundență crescută de Bifidobacteriaceae și Lactobacillaceae (plus Acidaminococcaeceae și Enterococaceae), însă care au raportat inconsistențe cu privire la celelate familii menționate în acest paragraf, precum și o abundență scăzută de Prevotellaceae, Clostridiaceae și Ruminococaceae (Nikolova et al., 2021).
Diferențe taxonomice la nivelul genurilor
Unii autori au arătat că genurile Anaerostipes, Blautia, Clostridium, Klebsiella, Lachnospiraceae incertae sedis, Parabacteroides, Parasutterella, Phascolarctobacterium și Streptococcus înregistrează o frecvență crescută (Cheung et al., 2019), alții indicând o astfel de creștere doar în cazul Paraprevotella (Sanada et al., 2020). O altă meta-analiză a indicat însă că frecvența de Anaerostipes, Blautia, Klebsiella, Paraprevotella și Phascolarctobacterium este inconsistentă, că numărul de Clostridium este unul redus și că frecvența de Parabacteroides și Streptococcus este ridicată (Nikolova et al., 2021).
Un număr scăzut de bacterii a fost înregistrat în cazul Bifidobacterium, Dialister, Escherichi-Shigella, Faecalibacterium și Ruminococcus (Cheung et al., 2019). Și alți cercetători au descoperit o frecvență redusă de Bifidobacterium, Escherichia-Shigella, Faecalibacterium și Ruminococcus, precum și de Caproccus (Sanda et al., 2020). Într-o altă meta-analiză aceste rezultate au fost parțial confirmate, cu niveluri scăzute de Dialister, Faecalibacterium și Caproccus și cu rezultate inconsistente pentru Bifidobacterium, Escherichia-Shigella și Ruminococcus (Nikolova et al., 2021).
În aceeași meta-analiză au fost identificate rezultate inconsistente și pentru Dorea, Roseburia, Oscillibacter, Gemmiger, Clostridium cl. IV, Clostridium cl. XI, Turicibacter, Eubacterium, Pavimonas, Megamonas, Actinomyces, Collinsella, Alistipes, Bacteroides și Haemophilius (Nikolova et al., 2021), o parte din aceste rezultate inconsistente (Roseburia, Oscilibacter, Megamonas, Alistipes și Bacteroides) fiind identificate și în altă recenzie sistematică (Cheung et al., 2019).
În final, au fost identificate niveluri crescute de Lachnoclostridium, Erysipelotrichaceae is., Holdemania, Megasphaera, Veillonella, Lactobacillus, Acidaminococcus, Enterococcus, Atopobium, Eggerthella și Olsenella, dar și niveluri scăzute de Fusicatenibacter, Subdoligranulum, Butyricicoccus, Eubacterium ventriosum, Odoribacter și Sutterella (Nikolova et al., 2021).
Cauzele acestor rezultate inconsistente
În prezent nu există dovezi pentru specificitatea depresiei [35], iar o parte dintre rezultatele inconcludente prezentate anterior ar putea fi explicate de doi factori: regiunea geografică și medicația psihiatrică (Nikolova et al., 2021). Regiunea geografică se referă de fapt la diferențele dietetice de natură geografică/etnică, precum și la diferențele genetice, imune și comportamentale specifice gazdelor care aparțin unei anumite populații și care pot afecta microbiomul intestinal în mod (in)direct (Cheung et al., 2019).
De exemplu, diferențele dietetice existente între culturile estice și cele vestice par să afecteze compoziția și diversitatea bacteriilor din microbiomul intestinal (ex. dietele care conțin cantități mari de grăsimi fiind asociate cu un număr mai mare de bacterii gram-negative care pot ulterior să crească concentrația de lipopolizaharide și să stimuleze sistemul imunitar) (Barandouzi et al., 2020).
Medicația psihiatrică se referă la tratamentul medicamentos pe care îl urmează o parte din persoanele care suferă de depresie. Unele dintre cele mai utilizate medicamente în acest caz sunt inhibitorii selectivi ai recaptării serotoninei. Aceștia din urmă au capacitatea de a afecta neuronii enterici, fiind caracterizați de proprietăți antibiotice care pot produce disbioză (Sjöstedt et al., 2021).
Efectele consumului de psihobiotice asupra simptomelor depresive
În prezent există o ipoteză conform căreia consumul de probiotice (psihobiotice) [36] ar putea avea efecte terapeutice la nivelul SNC prin îmbunătățirea integrității barierei gastrointestinale, ceea ce ar împiedica endotoxinele să pătrundă în circulația sanguină și implicit ar reduce inflamația din organism, reglând activitatea axei HHC și a neurotransmițătorilor (Wallace & Milev, 2017). Interesant este faptul că probioticele par să aibă efecte semnificative asupra stării mentale în cazul acelor persoane care manifestă simptome depresive, însă nu și în cazul persoanelor din grupurile de control (Nadeem et al., 2018).
Psihobioticele au capacitatea de a produce substanțe neuroactive care pot afecta axa intestin-creier în trei modalități diferite: a) efecte psihologice asupra proceselor emoționale și cognitive; b) efecte sistematice asupra axei HHC, asupra răspunsului la stres și a inflamației din organism; c) efecte neuronale asupra neurotransmițătorilor și proteinelor (ex. FNDC, glutamatul etc.) (Minayo et al., 2021).
De exemplu, rezultatele unei meta-analize care cuprinde un total de 1.349 de participanți au arătat că nu a existat nici o diferență semnificativă la nivelul simptomelor depresive între grupul experimental și cel placebo după intervenție, dar că indivizii care suferă de depresie ușoară/moderată au înregistrat îmbunătățiri semnificative în starea lor ca urmare a consumului de probiotice în comparație cu cei din grupul de control (Ng et al., 2018).
Aceste rezultate au fost (parțial) replicate în cadrul unei alte meta-analize care a arătat că prebioticele nu diferă de placebo în raport cu efectele pe care le produc asupra depresiei, dar că există un efect semnificativ (însă redus) asupra acesteia atunci când sunt consumate probiotice. De asemenea, efectul a fost unul mult mai puternic în cazul grupului clinic în comparație cu grupul de control (Liu et al., 2019).
O altă meta-analiză, de această dată realizată pe un eșantion de 1.901 participanți, a arătat că probioticele au avut efecte semnificative asupra simptomelor depresive ale persoanelor care suferă de TDM, dar că aceste efecte nu s-au păstrat și în cazul personelor care suferă de alte condiții clinice sau celor din populația generală (Goh et al., 2019).
Pe de altă parte, într-o meta-analiză mai recentă s-a descoperit faptul că prebioticele și probioticele moderează funcțiile căii kynureniene [37], mai precis că diminuează concentrația de kynurenină din serum și rația de kynunerină:triptofan, ceea ce se asociază cu diminuarea neuroinflamației și implicit cu o stare mentală mai bună (Purton et al., 2021).
Cauzele pentru care nu putem trage (momentan) concluzii definitive din aceste studii
Există mai multe motive pentru care rezultatele cu privire la efectele probioticelor asupra depresiei sunt inconcludente. Pentru început, noi nu cunoaștem în prezent care este durata, dozajul și tipul de probiotice care ar trebui administrate în cazul depresiei (Wallace & Milev, 2017). Studiile utilizate în meta-analizele ale căror rezultate le-am prezentat anterior se diferențiază unele de celelalte din punctul de vedere al regiunii geografice/medicației psihiatrice a participanților (unele dintre ele nici nu au controlat aceste variabile), precum și din alte considerente metodologice.
De exemplu, modul în care sunt consumate aceste probiotice diferă de la un studiu la celălalt (de la ingerarea de tablete, capsule și pudre, până la ingerarea de brânzeturi, iaurturi și lapte) iar acest lucru poate afecta direct calitatea și implicit eficiența lor – de obicei fiind necesară depozitarea la temperaturi joase pentru a spori supraviețuirea bacteriilor, ceea ce nu este întotdeauna valabil în cazul tabletelor de exemplu (Ng et al., 2018).
Utilizarea unor combinații diferite de tulpini de bacterii produce efecte diferite la nivelul stării mentale, întrucât pare că nu toate tipurile de bacterii sunt la fel de importante sau la fel de potente din acest punct de vedere (Nadeem et al., 2018). Introducerea unor studii care au avut eșantioane compuse din participanți cu diferite forme de tulburări depresive și de boli fiziologice poate fi încă un motiv pentru care rezultatele meta-analizelor respective sunt (parțial) inconcludente (Goh et al., 2019), la fel ca și utilizarea unor diferite scale de măsurare a simptomatologiei depresive (Wallace & Milev, 2017).
Concluzii
Există mai multe concluzii pe care le putem trage din informațiile prezentate în acest articol. În primul rând, că există o relație directă între compoziția bacteriană a microbiomului intestinal uman și depresie. Axa intestin-creier permite comunicarea directă a microbiomului intestinal cu SNC prin intermediul semnalizării imune, endocrine și nervoase, astfel încât procesele cerebrale pot influența procesele gastrointestinale și invers. În al doilea rând, intervenția medicală în cazul depresiei ar trebui să aibă în vedere și modalități de optimizare a microbiomului intestinal prin intermediul nutriției și/sau a suplimentelor alimentare. Consumul de alimente care conțin prebiotice și probiotice poate îmbunătăți starea persoanelor care suferă de depresie și poate contribui la vindecarea lor.
În al treilea rând, există o conexiune profundă între dimensiunea psihică și cea fizică a ființei umane astfel încât este extrem de probabil ca orice formă de tulburare psihică să fie asociată cu modificări la nivel fiziologic și orice boală fizică să fie asociată cu modificări la nivel psihologic. În al patrulea rând, metodologiile actuale de cercetare științifică necesită îmbunătățite și actualizate în conformitate cu nevoia de a studia ființa umană într-un mod holist. Crearea unor echipe multidisciplinare de cercetare și intervenție terapeutică ar trebui să devină un imperativ real, dincolo de cuvintele pompoase din manuale, asta dacă ne dorim să ne apropiem cât mai mult de posibilitatea de a găsi modalități de a trata ființa umană în mod real și nu doar în superficialitatea simptomelor.
Cum să cităm?
Vă rugăm să citați acest articol în felul următor: Mihai, R.-A. (2022, Iulie 13). Intestine deprimate: rolul bacteriilor microbiomului intestinal în apariția și tratamentul depresiei. Retrieved from Lumen in mundo: https://lumeninmundo.com/2022/07/13/intestine-deprimate-rolul-bacteriilor-microbiomului-intestinal-in-aparitia-si-tratamentul-depresiei/
Note
[1] Pentru o explicație detaliată a modalității de funcționare a axei HHC vă sugerez să citiți acest articol (subcapitolul „Axa hipotalamo-hipofizo-corticosuprarenală”) sau acest articol (subcapitolul „Experiențele adverse din copilărie pot altera funcțiile sistemelor de gestionare a stresului”).
[2] Pare că gradul de dereglare a modalității de funcționare a axei HHC diferă în funcție de vârstă: persoanele tinere înregistrează niveluri mai scăzute de cortisol, cotricotropină și hormoni eliberatori de corticotropină în comparație cu persoanele vârstnice (Murri et al., 2014).
[3] Nivelurile scăzute de FNDC și de monoamine se asociază cu o plasticitate sinaptică redusă ca urmare a blocării receptorilor N-metil-D-aspartat (i.e., un tip major de receptori de glutamat implicați în transmiterea sinaptică), iar plasticitatea sinaptică redusă este asociată cu apariția depresiei (Unal & Moustafa, 2021).
[4] Histonele sunt proteine alcaline care se regăsesc în nucleul celulelor eucariote și care unesc acidul dezoxiribonucleilc în cromatină și în cromozomi.
[5] Investigarea modificărilor care apar în microbiomul intestinal în cazul depresiei este o abordare recentă, cele mai multe articole care vizează acest subiect fiind publicate începând cu perioada anilor 2008-2009 (Khanna & Tosh, 2014).
[6] Estimarea prevalenței depresiei este dificilă în special din cauza diferențelor metodologice de la nivelul studiilor care se ocupă de acest subiect. Rezultatele unei meta-analize (Levis et al., 2019) care a inclus un total de 69 de studii (81 de estimări ale prevalenței) au arătat că prevalența depresiei variază în funcție de metoda de evaluare utilizată și că în cele mai multe dintre cazuri se vorbește despre prevalența depresiei/tulburărilor depresive deși studiile respective nu evaluează tulburările depresive în sine (nu pot vorbi despre prezența unui diagnostic), ci mai degrabă simptomatologia depresivă. Din acest motiv există posibilitatea ca (o parte din) estimările referitoare la prevalența depresiei în lume să fie greșite.
[7] Acest lucru pare să se datoreze diferențelor biologice dintre cele două sexe mai degrabă decât rasei, culturii, dietei, educației sau altor factori socioeconomici (Albert, 2015).
[8] Pentru a înțelege mai clar distincția dintre microbiotă și microbiom vă sugerez să verificați figura nr. 2 din articolul lui Berg et al. (2020), pe care o puteți vedea aici.
[9] Există autori care sunt de părere că împărțirea microorganismelor în benefice și patogene este relevantă doar în unele contexte de cercetare și că o abordare mult mai apropiată de realitate este cea holistică așa cum o postulează teoria evoluției hologenomului conform căreia starea de sănătate a gazdei este întreținută de interacțiunea benefică cu propriul microbiom, in timp ce apariția efectelor patogene este asociată cu disbioza (i.e., dereglarea homeostaziei microbiotei prin modificări ale conținutului, funcțiilor, activităților metabolice sau amplasării microorganismelor care o compun – în sensul de localizare în diferite regiuni ale tractului gastrointestinal) (Berg et al., 2020).
[10] Bacteriocinele sunt toxine proteice sau peptidice implicate în inhibarea procesului de creștere a tulpinilor bacteriene similare.
[11] Peptidele antimicrobiene sunt molecule naturale care sunt produse de către organismele multicelulare ca prim răspuns defensiv la contactul cu agenții patogeni.
[12] Citokinele sunt proteine solubile care sunt eliberate de celulele din organism și care mediază și reglează răspunsurile imune și inflamatorii.
[13] Proteinele de fază acută sunt proteine produse de ficat atunci când organismul se confruntă cu o infecție/inflamație și care își modifică concentrațiile din sânge ca răspuns la citokinele proinflamatorii.
[14] Fibrele viscerale aferente sunt responsabile de transmiterea informațiilor referitoare la modificările locale din mediul chimic și mecanic al organelor.
[15] În cazul semnalelor aferente viscerale care provin din intestine și care ajung în trunchiul cerebral și în talamus se poate vorbi doar uneori de o percepție conștientă, cu toate că există posibilitatea ca semnalele respective să poată fi înregistrate în mod subliminal (Ford & Talley, 2021). De obicei semnalele respective devin mult mai vizibile în cazul unor boli de natură gastrointestinală.
[16] SNE este o rețea de neuroni care se regăsește în interiorul peretelui tractului gastrointestinal.
[17] SNE este compus din aproximativ 500 de milioane de neuroni și poate acționa independent de SNC, fiind considerat un al doilea creier al organismului uman (Misiak et al., 2020).
[18] Axa HHC este extrem de sensibilă la prezența factorilor stresori și nu poate face distincția între stresul real și cel perceput. Experiențele puternic stresante (precum traumele), în special cele de pe parcursul copilăriei și adolescenței, au capacitatea de a altera modalitatea de funcționare a acestei axe și de a produce hiper/hipocortisolism la nivelul organismului. Pentru mai multe detalii referitoare la subiectul respectiv vă invit să citiți acest articol.
[19] IL-6 este produsă de limfocite, monocite, macrofage sau de celulele din țesuturi ori din SNC – implicată în medierea răspunsurilor imune și inflamatorii ale organismului.
[20] IL-1β se ocupă de reglarea răspunsului imun și inflamator, fiind implicată în reacția de fază acută, în casexie și în febră.
[21] TNF-α este o citokină proinflamatorie care joacă un rol important în semnalizarea celulară și care are capacitatea de a distruge celulele tumorale.
[22] Th1 sunt celule ale sistemului imunitar care sunt implicate în reacția imunității mediată celular.
[23] Chemokinele sunt molecule chemotactice care au rol de mediatori în răspunsul inflamator al sistemului umunitar.
[24] IL-8 are rolul de a aduna neutrofilele în regiunile afectate ale corpului.
[25] IL-10 este implicată în procesul antiinflamator și imunosupresor.
[26] TGF-β contribuie la formarea de noi vase de sânge, la reglarea răspunsului imun și la vindecarea rănilor.
[27] Joncțiunile strânse constituie o barieră intercelulară care există între celulele epiteliale din tractul gastrointestinal și ficat.
[28] Endotoxinele sunt o componentă a peretelui celular extern al bacteriilor gram-negative care ajung să fie eliberate în circulația sanguină atunci când bacteriile respective sunt distruse, având un rol important în stabilitatea peretelui celular.
[29] Bacteria Escherichia coli (E. coli) poate produce o proteină numită ClpB care imită hormonul stimulator al α-melanocitului. Acesta din urmă determină eliberarea de proopiomelancortină care determină la rândul ei eliberarea de hormon adrenocorticotropic (vezi nota [1] pentru mai multe explicații referitoare la implicația acestui hormon în activitatea axei HHC).
[30] Triptofanul este un aminoacid esențial care este precursorul serotoninei.
[31] Levodopa este un aminoacid neesențial care este sintetizat de organismul uman.
[32] Enterocitele sunt celule care acoperă suprafața internă a intestinului gros și a intestinului subțire, fiind implicate în procesul de absorbție.
[33] Una dintre cele mai uimitoare descoperiri în acest caz constă în faptul că transplantul de materii fecale de la persoane care suferă de TDM la șoareci de laborator care au fost a priori tratați cu antibiotice a produs în aceștia apariția unor manifestări specifice fenotipului depresiv, precum și faptul că transplantul de fecale de la persoane sănătoase la persoane care suferă de TDM a produs o îmbunătățire a simptomelor depresive în acestea de urmă pentru o anumită perioadă (de la 12 săptămâni până la 17 luni) (Meyyappan et al., 2020).
[34] Există o frecvență crescută de tulburări psihice, în special de anxietate și depresie, în cazul persoanelor care suferă de boli gastrointestinale (Simpson et al., 2020a).
[35] Pare totuși că anumite tulburări psihice împărtășesc același tipar de modificări la nivelul microbiomului intestinal (Nikolova et al., 2021).
[36] Pentru o înțelegere ușoară e important să știți că probioticele se referă la anumite microorganisme care au efecte benefice la nivel gastroitestinal (și nu numai, după câte puteți vedea) atunci când sunt ingerate, în timp ce prebioticele se referă la fibre care stimulează creșterea bacteriilor benefice din intestine. Termenul de psihobiotice este utilizat de obicei în cercetări cu scopul de a face referire la organismele vii care odată ce sunt ingerate pot produce efecte benefice la nivelul stării de sănătate a persoanelor care suferă de tulburări psihice. Pentru o înțelegere mai specializată a acestor termeni vă sugerez totuși să citiți articolul scris de Zendeboodi et al. (2020).
[37] Calea kynureninei constituie principala cale de degradare a triptofanului. Mai precis, citokinele de tipul interferon-r (IFN-R) (implicat în răspunsul imun), IL-1β și IL-6 pot induce producția de indolamină 2,3-dioxigenază 1 (IDO-1) și triptofan 2,3-dioxigenază (TDO) ce constituie principalele enzime implicate în degradarea triptofanului. Aceste enzime pot activa calea kynureninei care poate reduce cantitatea de triptofan și sinteza serotoninei (Park & Hong, 2018).
Activarea căii kynureniene poate duce la formarea metaboliților kynurieni neurotoxici, precum acidul quinolinic (agonist al receptorilor NMDA), care intensifică inflamația din creier și care conduce la hiperactivarea glutamatergică a neurotransmițătorilor (Dantzer, 2017).
Pe lângă acidul quinolinic există și un acid kynurenic (tot un metabolit principal al kynureninei) care are rol neuroprotectiv. Apariția ideației suicidare și a tentativelor de suicid pare să fie legată de dezechilibrul care se produce la nivel neuronal între acidul quinolinic și acidul kynurenic. Persoanele care au avut tentative de suicid au înregistrat niveluri și de 300% mai mari de acid quinelinic în comparație cu grupurile de control, acest nivel rămânând la jumătate (150%) chiar și la doi ani după tentativa de suicid (Park & Hong, 2018).
Surse bibiliografice:
Albert, P. R. (2015). Why is depression more prevalent in women? Journal of Psychiatry and Neuroscience, 40(4), 219-221, doi: 10.1503/jpn.150205.
American Psychiatric Association. (2016). DSM-5: Manual de Diagnostic și Clasificare Statistică a Tulburărilor Mintale. București: Editura Medicală Callisto.
American Psychological Association. (2015). APA Dictionary of Psychology. Washington, DC: American Psychological Association.
Armugam, M., Raes, J., Pelletier, E., Le Paslier, D., Yamada, T., Mende, D. R., . . . Bork, P. (2011). Enterotypes of the human gut microbiome. Nature, 473(7346), 174-180, doi: 10.1038/nature09944.
Barandouzi, Z. A., Starkweather, A. R., Henderson, W. A., Gyamfi, A., & Cong, X. S. (2020). Altered Composition of Gut Microbiota in Depression: A Systematic Review. Frontiers in Psychiatry, 11(541), doi: 10.3389/fpsyt.2020.00541.
Berg, G., Rybakova, D., Fischer, D., Cernava, T., Vergès, M.-C. C., Charles, T., . . . Schloter, M. (2020). Microbiome definition re-visited: old concepts and new challenges. Microbiome, 8(103), doi: 10.1186/s40168-020-00875-0.
Bueno-Notivol, J., Gracia-García, P., Olaya, B., Lasheras, I., López-Antón, R., & Santabárbara, J. (2021). Prevalence of depression during the COVID-19 outbreak: A meta-analysis of community-based studies. Psychology, 21(1), doi: 10.1016/j.ijchp.2020.07.007.
Cheung, S., Goldenthal, A. R., Uhlemann, A.-C., Mann, J. J., Miller, J. M., & Sublette, M. E. (2019). Systematic Review of Gut Microbiota and Major Depression. Frontiers in Psychology, 10(34), doi: 10.3389/fpsyt.2019.00034.
COVID-19 Mental Disorders Collaborators. (2021). Global prevalence and burden of depressive and anxiety disorders in 204 countries and territories in 2020 due to the COVID-19 pandemic. The Lancet, 398(10312), 1700-1712, doi: 10.1016/S0140-6736(21)02143-7.
Daniels, K. J., Koopman, M., & Aidy, E. S. (2017). Depressed gut? The microbiota-diet-inflammation trialogue in depression. Current Opinion in Psychiatry, 30(5), 369-377, doi: 10.1097/YCO.0000000000000350.
Dantzer, R. (2017). Role of the kynurenine metabolism pathway in inflammation-induced depression – Preclinical approaches. Current Topics in Behavioral Neurosciences, 31, 117-138, doi: 10.1007/7854_2016_6
Evrensel, A., & Ceylan, E. M. (2018). Gut-Microbiota-Brain Axis and Depression. În Y.-K. Kim, Understanding Depression. Volume 1. Biomedical and Neurobilogical Backround (pg. 197-207). Singapore: Springer.
Ford, A. C., & Talley, N. J. (2021). Irritable Bowel Syndrome. În M. Feldman, L. S. Friedman, L. J. Brandt, R. Chung, D. T. Rubin, & C. M. Wilcox, Sleisenger and Fordtran`s Gastrointestinal and Liver Disease (pg. 2008-2020). Philadelphia: Elsevier.
Goh, K. K., Liu, Y.-W., Kuo, P.-H., Chung, Y.-C. E., Lu, M.-L., & Chen, C.-H. (2019). Effect of probiotics on depressive symptoms: A meta-analysis of human studies. Psychiatry Research, 282, doi: 10.1016/j.psychres.2019.112568.
Khanna, S., & Tosh, P. K. (2014). A Clinician`s Primer on the Role of the Microbiome in Human Health and Disease. Mayo Clinic Proceedings, 89(1), 107-114, doi: 10.1016/j.mayocp.2013.10.011 .
Lam, W. R. (2018). Epidemiology and burden. În W. R. Lam, Depression (pg. 4-9). Oxford: Oxford University Press.
Lazary, J., Miezah, D., Moustafa, A. A., & Kéri, S. (2021). Peripheral biomarkers in major depressive disorders. În A. A. Moustafa, The Nature of Depression (pg. 3-16). Londra: Academic Press.
Leonard, B. E. (2018). Chronic Inflammation and Resulting Neuroprogression in Major Depression. În Y.-K. Kim, Understanding Depression. Biomedical and Neurobiological Backround. Volume 1 (pg. 191-196). Singapore: Springer.
Levis, B., Yan, X. W., He, C., Sun, Y., Benedetti, A., & Thombs, B. D. (2019). Comparison of depression prevalence estimates in meta-analyses based on screening tools and rating scales versus diagnostic interviews: a meta-research review. BMC Medicine, 17(65), doi: 10.1186/s12916-019-1297-6.
Lim, G. Y., Tam, W. W., Lu, Y., Ho, C. S., Zhang, M. W., & Ho, R. C. (2018). Prevalence of Depression in the Community from 30 Countries between 1994 and 2014. Nature, 8(2861), doi: 10.1038/s41598-018-21243-x.
Liu, R. T., Walsh, R. F., & Sheehan, A. E. (2019). Prebiotics and probiotics for depression and anxiety: A systematic review and meta-analysis of controlled clinical trials. Neuroscience and Biobehavioral Reviews, 102, 13-23, doi: 10.1016/j.neubiorev.2019.03.023.
Marchesi, J. R., & Ravel, J. (2015). The vocabulary of microbiome research: a proposal. Microbiome, 3(31), doi: 10.1186/s40168-015-0094-5.
Meyyappan, A. C., Forth, E., Wallace, C. J., & Milev, R. (2020). Effect of fecal microbiota transplant on symptoms of psychiatric disorders: a systematic review. BMC Psychiatry, 20(299), doi: 10.1186/s12888-020-02654-5.
Mikulska, J., Juszczyk, G., Gawrońska-Grzywacz, M., & Herbet, M. (2021). HPA Axis in the Pathomechanism of Depression and Schizophrenia: New Therapeutic Strategies Based on Its Participation. Brain Sciences, 11(10), doi: 10.3390/brainsci11101298.
Minayo, M. d., Miranda, I., & Telhado, R. S. (2021). A systematic review of the effects of probiotics on depression and anxiety: an alternative therapy? Ciencia e Saude Coletiva, 26(9), 4087-4099, doi: 10.1590/1413-81232021269.21342020.
Misiak, B., Loniewski, I., Marlicz, W., Frydecka, D., Szulc, A., Rudzki, L., & Samochowiec, J. (2020). The HPA axis dysregulation in severe mental illness: Can we shift the blame to gut microbiota? Progress in Neuropsychopharmacology & Biological Psychiatry, 102, doi: 10.1016/j.pnpbp.2020.109951.
Murri, M. B., Pariante, C., Mondelli, V., Masotti, M., Atti, A. R., Mellacqua, Z., . . . Amore, M. (2014). HPA axis and aging in depression: systematic review and meta-analysis. Psychoneuroendocrinology, 41, 46-62, doi: 10.1016/j.psyneuen.2013.12.004.
Nadeem, I., Rahman, M. Z., Ad-Dab`bagh, Y., & Akhtar, M. (2018). Effect of probiotic interventions on depressive symptoms: A narrative review evaluating systematic reviews. Psychiatry and Clinical Neurosciences, 73(4), 154-162, doi: 10.1111/pcn.12804/full.
Ng, X. Q., Peters, C., Ho, C. Y., Yutong, D. L., & Yeo, W.-S. (2018). A Meta-Analysis of the Use of Probiotics to Alleviate Depressive Symptoms. Journal of Affective Disorders, 1(228), 13-19, doi: 10.1016/j.jad.2017.11.063.
Nikolova, V. L., Hall, M. R., Hall, L. J., Cleare, A. J., Stone, J. M., & Young, A. H. (2021). Perturbations in Gut Microbiota Composition in Psychiatric Disorders. A Review and Meta-analysis. JAMA Psychiatry, 78(12), 1343-1354, doi: 10.1001/jamapsychiatry.2021.2573.
Park, S., & Hong, P. J. (2018). Suicidal Behavior in Depression: A Severe Form of Depression or a Distinct Psychobiology? În Y.-K. Kim, Understanding Depression. Volume 2. Clinical Manifestations, Diagnosis and Treatment (pg. 143-150). Singapore: Springer.
Purton, T., Staskova, L., Lane, M. M., Dawson, S. L., West, M., Firth, J., . . . Marx, W. (2021). Prebiotic and probiotic supplementation and the tryptophan-kynurenine pathway: A systematic review and meta analysis. Neuroscience and Biobehavioral Reviews, 123, 1-13, doi: 10.1016/j.neubiorev.2020.12.026.
Rinniella, E., Raoul, P., Cintoni, M., Franceschi, F., Miggiano, G. A., Gasbarrini, A., & Mele, M. C. (2019). What is the Healthy Gut Microbiota Composition? A Changing Ecosystem across Age, Environment, Diet, and Diseases. Microorganisms, 7(1), doi: 10.3390/microorganisms7010014.
Salk, R. H., Hyde, J. S., & Abramson, L. Y. (2017). Gender Differences in Depression in Representative National Samples: Meta-Analyses of Diagnoses and Symptoms. Psychological Bulletin, 143(8), 783-822, doi: 10.1037/bul0000102.
Sanada, K., Nakajima, S., Kurkowa, S., Barceló-Soler, A., Ikuse, D., Hirata, A., . . . Kishimoto, T. (2020). Gut microbiota and major depressive disorder: A systematic review and meta-analysis. Journal of Affective Disorders, 266, 1-13, doi: 10.1016/j.jad.2020.01.102.
Simpson, C. A., Diaz-Arteche, C., Eliby, D., Schwartz, O. S., Simmons, J. G., & Cowan, C. S. (2020b). The gut microbiota in anxiety and depression – A systematic review. Clinical Psychology Review, 83, doi: 10.1016/j.cpr.2020.101943.
Simpson, C. A., Mu, A., Haslam, N., Schwartz, O. S., & Simmons, J. G. (2020a). Feeling down? A systematic review of the gut microbiota in anxiety/depression and irritable bowel syndrome. Journal of Affective Disorders, 266, 429-446, doi: 10.1016/j.jad.2020.01.124.
Sjöstedt, P., Enander, J., & Isung, J. (2021). Serotonin Reuptake Inhibitors and the Gut Microbiome: Significance of the Gut Microbiome in Relation to Mechanism of Action, Treatment Response, Side Effects, and Tachyphylaxis. Frontiers in Psychiatry, 12, doi: 10.3389/fpsyt.2021.682868.
Strandwitz, P. (2018). Neurotransmitter modulation by the gut microbiota. Brain Research, 15(1693), 128-133, doi: 10.1016/j.brainres.2018.03.015.
Sun, H., Kennedy, P., & Nestler, E. (2013). Epigenetics of the Depressed Brain: Role of Histone Acetylation and Methylation. Neuropsychopharmacol, 38, 124-137, doi: 10.1038/npp.2012.73.
Thursby, E., & Juge, N. (2017). Introduction to the human gut microbiota. Biochemical Journal, 474(11), 1823-1836, doi: 10.1042/BCJ20160510.
Unal, G., & Moustafa, A. A. (2021). The neural substrates of different depression symptoms: Animal and human studies. În A. A. Moustafa, The Nature of Depression (pg. 59-79). Londra: Academic Press.
Wallace, C. J., & Milev, R. (2017). The effects of probiotics on depressive symptoms in humans: a systematic review. Annals of General Psychiatry, 16(14), doi: 10.1186/s12991-017-0138-2.
World Health Organization. (2021, June 17). Suicide. Preluat de pe World Health Organization: https://www.who.int/news-room/fact-sheets/detail/suicide
Zendeboodi, F., Khorshidian, N., Mortazavian, A. M., & da Cruz, A. G. (2020). Probiotic: conceptualization from a new approach. Current Opinion in Food Science, 32, 103-123, doi: 10.1016/j.cofs.2020.03.009.
Zhang, K., Huang, J., Feng, J., Zhang, H., & Tian, M. (2018). Structural, Functional, and Molecular Neuroimaging in Depression. În Y.-K. Kim, Understanding Depression. Biomedical and Neurobiological Backround. Volume 1 (pg. 131-143). Singapore: Springer.
Cum să cităm?
Vă rugăm să citați acest articol în felul următor: Mihai, R.-A. (2022, Iulie 13). Intestine deprimate: rolul bacteriilor microbiomului intestinal în apariția și tratamentul depresiei. Retrieved from Lumeninmundo: https://lumeninmundo.com/2022/07/intestine-deprimate-rolul-bacteriilor-microbiomului-intestinal-in-aparitia-si-tratamentul-depresiei/








De mult n-am mai citit ceva scris cu atâta seriozitate.
Într-o societate superficială precum este cea din prezent e necesar să ne (re)amintim importanța tratării cu seriozitate a suferinței umane.
Pingback: Despre calitatea jurnalismului științific din România (Episodul 2: Bacteriile din intestine și tulburarea din spectrul autist) | lumeninmundo